RNA疫苗或成新冠的终结者?
RNA疫苗或成新冠的终结者?RNA疫苗的实际产能与预期可能会有偏差。撰文 | 汪汪11月9日,美国辉瑞(Pfizer)公司发布消息,称其与德国BioNTech公司合作研发的mRNA
RNA疫苗的实际产能与预期可能会有偏差。
撰文 | 汪汪
11月9日,美国辉瑞(Pfizer)公司发布消息,称其与德国BioNTech公司合作研发的mRNA新冠疫苗BNT162b2对没有感染新冠病毒的健康受试者有效,且有效性超过90%。紧随其后,11月16日,Moderna公布了该公司研发的新冠疫苗mRNA-1273 的三期临床试验结果,表明该疫苗具有94.5%的保护效力。这两则新闻都引起了巨大的轰动。目前全世界有超过200种COVID-19疫苗正处于研发中,其中48种已经进入临床研究阶段[1]。全球新冠感染人数还在不断增加,所有人都将期盼的目光转向疫苗,它或许是破局的唯一途径。各大公司和科研机构都在快马加鞭, RNA疫苗为何能够拔得头筹?
五类疫苗,各有优势
早在1880年以前,人类就已经开发出疫苗,用于预防致病微生物,英语中疫苗一词“vaccine”源自于爱德华·金纳(Edward Jenner)所使用的牛痘,“vacca”即是拉丁文中的“牛”。牛痘疫苗成功消除了当时肆虐人间的天花,爱德华也因此被称为疫苗之父。在此之后,人类继续成功地用疫苗控制和根除了许多严重的动物传染病(例如经典的猪瘟、牛瘟)和人类传染病,如小儿麻痹症、麻疹、腮腺炎、流感等[2]。
疫苗的种类不同,但发挥作用的机制是相似的。它们通常采用注射形式,将低剂量的病原体注入人体——这些病原体可能是部分也可能是全部形态——以促使人体产生针对这种病原体的抗体。抗体具有免疫记忆特性,当再次出现相同的病原时,机体会迅速产生免疫响应,进而预防感染。
根据引发免疫应答的方式不同,我们可以将制备疫苗的技术分为五种(图1)。一些技术比如说减毒活疫苗、灭活疫苗等已经投入大规模应用,而一些新技术比如RNA/DNA疫苗还从未出现于人用商业疫苗中。
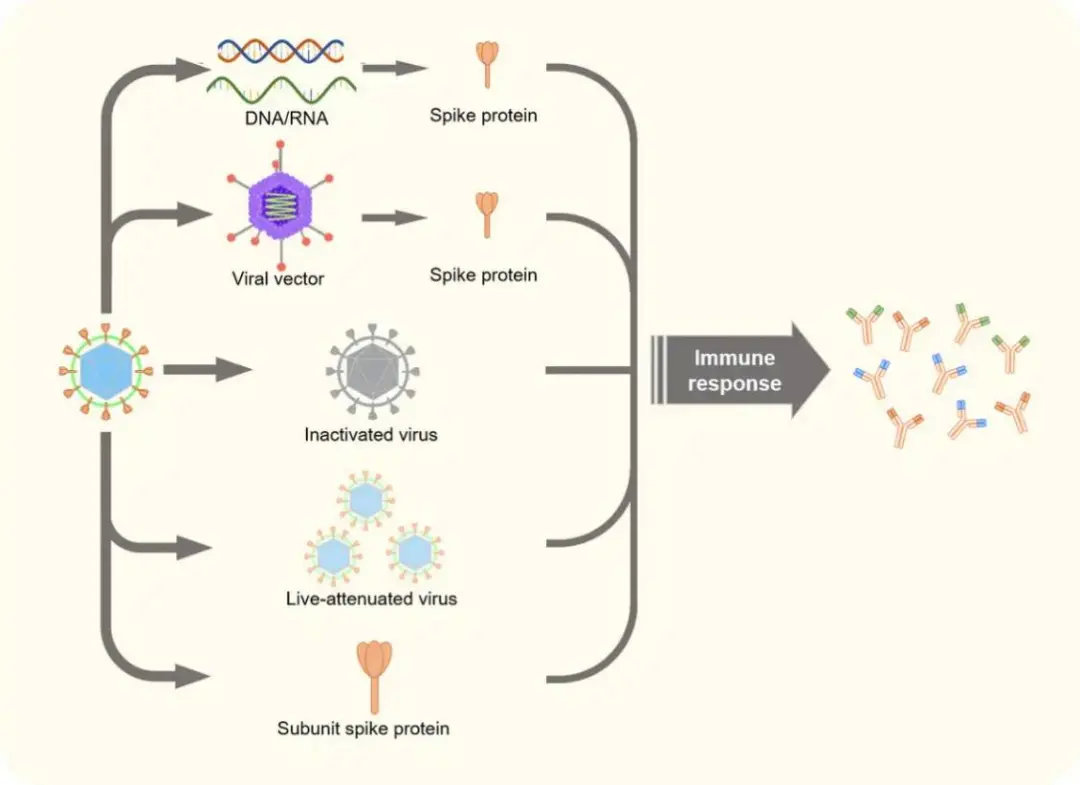
图1. 五种类型疫苗通过引发免疫应答的方式不同而有所区别[3]
1. 减毒活疫苗(Live attenuated vaccines)
减毒活疫苗是现有的最为成功的疫苗,在抗传染病战场上曾立下战功无数,例如预防麻疹、脊髓灰质炎。减毒活疫苗是从自然界筛选或者由实验室培育出的毒力降低或者无毒的病原体,这些病原体可以存活但不会引起疾病,接种后,疫苗中的病毒可以生长、复制,从而引起接种者的免疫反应。
优点:
模仿自然感染过程,因此具有强大的保护作用
具有成熟的监管批准体系,以及大规模制造的经验
单次注射即可发挥免疫效应,无需其他佐剂
缺点:
活病毒仍然有微小的可能会在人体内恢复毒力
由于潜在的安全隐患,免疫系统较弱的人被限制使用
需冷藏储存,给运输带来潜在压力
2. 灭活疫苗( Inactivated vaccines)
灭活疫苗是通过加热、化学手段或者辐射等方式使病毒失去活性,这些灭活后的病毒无法在体内复制,但仍可触发免疫效应。灭活疫苗也被广泛使用,早前在针对脊髓灰质炎病毒的疫苗和某些类型的流感疫苗中曾应用过这一技术。九月初,中国政府已经紧急批准了由Sinovac Biotech公司开发的灭活COVID-19疫苗,限量使用于高危人群[4]。
优点:
技术完备,安全性高
病毒经过灭活,可用于免疫力低下的人群
缺点:
免疫性低,需要多次接种加强免疫。
3. 蛋白亚单位疫苗(Protein subunit)
亚单位疫苗不包含病毒的活成分,而是由可触发免疫反应的病毒纯化片段(如蛋白质抗原)制成。这也是一种此前使用过的技术,如乙型肝炎疫苗就是以乙型肝炎病毒表面抗原为基础制成的。
优点:
没有病毒活成分,安全性较高
可用于免疫力低下的人群和其他弱势人群
缺点:
需要对能引起免疫反应的蛋白质抗原进行研究,因此研发时间较长
免疫性低,需要多次接种加强免疫,或与免疫系统刺激剂同时使用
4. 载体病毒疫苗(Virus vectors)
此类疫苗通常采用被削弱且本身无法引起疾病的病毒作为载体,将真正的致病抗原传递到体内,在感染体内细胞后,载体病毒携带的大量抗原可以引发免疫反应,继而产生免疫效果。本次疫情中一个引人注目的例子是澳大利亚政府寄予厚望的一颗疫苗:由牛津大学与阿斯利康联合研发的疫苗AZD1222(以前称为ChAdOx1),它就是基于改良的黑猩猩腺病毒作为载体的疫苗。
国际上目前已批准为两种基于腺病毒载体的COVID-19疫苗开启紧急使用,在医务人员、防疫人员、边检人员以及保障城市基本运行人员等特殊人群中,先建立起免疫屏障,保障整个城市的运行。一个是由中国军事医学科学院与CanSino Biologics公司联合研发的疫苗[5],另一个是由隶属俄罗斯卫生部的加马列亚研究中心(Gamaleya Research Institute)研发的疫苗[6]。
优点:
免疫效果好,疫苗接种后可以实现抗体的高浓度表达
单剂量足以刺激长期保护
缺点:
载体病毒也可能激发免疫应答,从而降低疫苗的有效性
生产效率较低,成本较高
5. DNA/RNA 疫苗 (DNA/RNA-based)
DNA和RNA疫苗是在对病毒进行基因测序后,找到编码一部分病毒遗传物质的片段(例如刺突蛋白),通过在实验室制造这些片段来生产疫苗。在注射疫苗后,人类的细胞会通过这些片段来产生该病毒的对应部分蛋白(或抗原),进而激发免疫反应。此类疫苗仅需要病毒的基因序列即可快速进行研发,所以它们能率先进入临床试验。例如Moderna公司和美国国家过敏和传染病研究所(US National Institute of Allergy and Infectious Diseases)共同开发的RNA疫苗mRNA-1273,在新冠病毒测序后仅两个月就进入了临床试验阶段。
优点:
仅根据基因测序即可快速开展疫苗研发
制造技术简单,可以大规模生产,成本相对低廉
仅含病毒的遗传物质片段,不会使人感染病毒
缺点:
目前尚无批准用于人类的DNA / RNA疫苗,因此在批准使用之前,它们可能会面临难度更大的法规审查
病毒片段带来的免疫效果低,因此可能需要多次接种加强免疫
理论上仍存在这样一种可能性:疫苗中所含的DNA/RNA片段可能被整合进入接种者基因组中
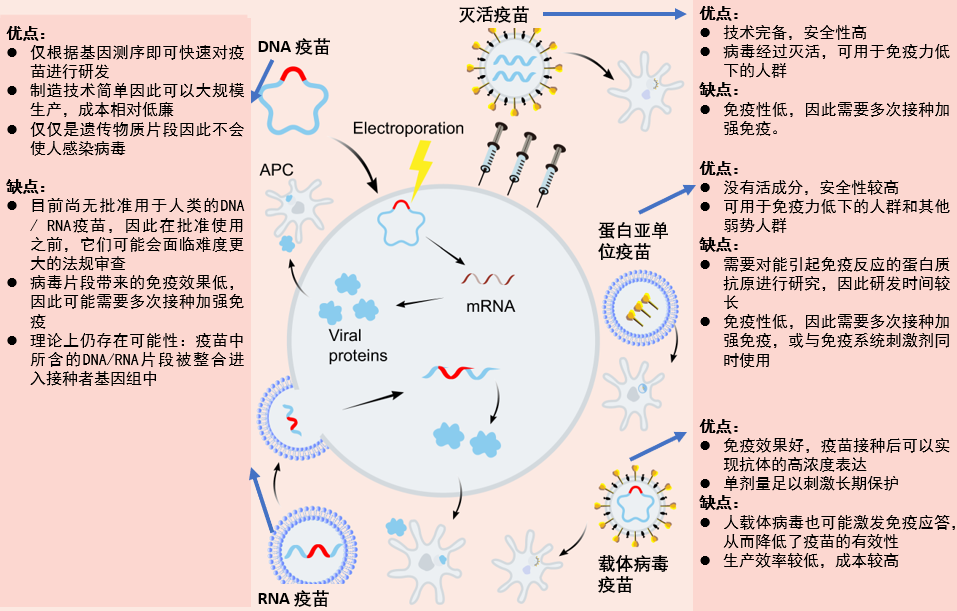
图2. 各种疫苗及其潜在优点和缺点的总结
(原图来源:https://www.nature.com/articles/s41392-020-00352-y)
RNA疫苗:美景尚未成真
11月9日,辉瑞(Pfizer)公司和BioNTech公司联合宣布,双方联合开发的基于mRNA技术的候选新冠疫苗BNT162b2在三期临床试验的中期有效性分析中,显示出高达90%的保护效力。据《金融时报》(Financial Times)报道,如一切顺利,辉瑞计划在11月的第三周申请紧急批准上市[7]。紧随其后,11月16日,Moderna公布了该公司COVID-19疫苗mRNA-1273 的三期临床试验结果,数据表明该疫苗具有94.5%的保护效力,根据这一结果,Moderna将在未来几周向FDA申请紧急授权(EUA)[8]。
RNA疫苗为何能在此次全球新冠疫苗研发竞赛中遥遥领先?
mRNA(信使核糖核酸)是一种储存着遗传信息的RNA分子,在人体内,它由DNA转录而来,可以为细胞提供指令,指导细胞合成对应蛋白。一言以蔽之,mRNA疫苗的作用机制就是让人体细胞表达病毒蛋白片段,从而激发免疫反应(图3)。
制备mRNA疫苗,首先要在对病毒进行遗传物质分析后,找到病毒编码特异性抗原的mRNA序列。例如面对新冠病毒,我们需要找到编码表面刺突蛋白的对应序列——因为这是病毒结构中最可能引起人类免疫反应的病毒部分。然后构建疫苗。
目前有两种mRNA疫苗形式:非复制mRNA(NRM)疫苗和自扩增mRNA(SAM)疫苗。构建好的mRNA被配制进载体中——通常是脂质纳米颗粒——以保护它们免受降解,并促进细胞摄取。载体颗粒被摄取进入细胞后,释放出mRNA,被核糖体翻译后产生目标蛋白质(可被识别的抗原)。目标蛋白被细胞分泌后,被免疫系统识别并激发免疫反应[9]。
在上文中我们提到,典型的疫苗是用灭活、减毒或者是微生物片段来生产的,是由外界递入的蛋白片段或者由外界递入的病毒产生的蛋白片段,来直接激发人体的免疫应答。而mRNA疫苗从第一步开始就截然不同,它必须被人体细胞吸收,然后诱导人体细胞产生部分病毒蛋白,这些病毒蛋白根据mRNA的序列而表达。传统疫苗就像是给人体输送了一台可以表达病毒蛋白的计算机,而mRNA疫苗更像是赋予人体一套操作系统,由人体自行表达蛋白,这些蛋白分子是独立的,并不会组装成病毒,但是可以引发免疫应答[10]。
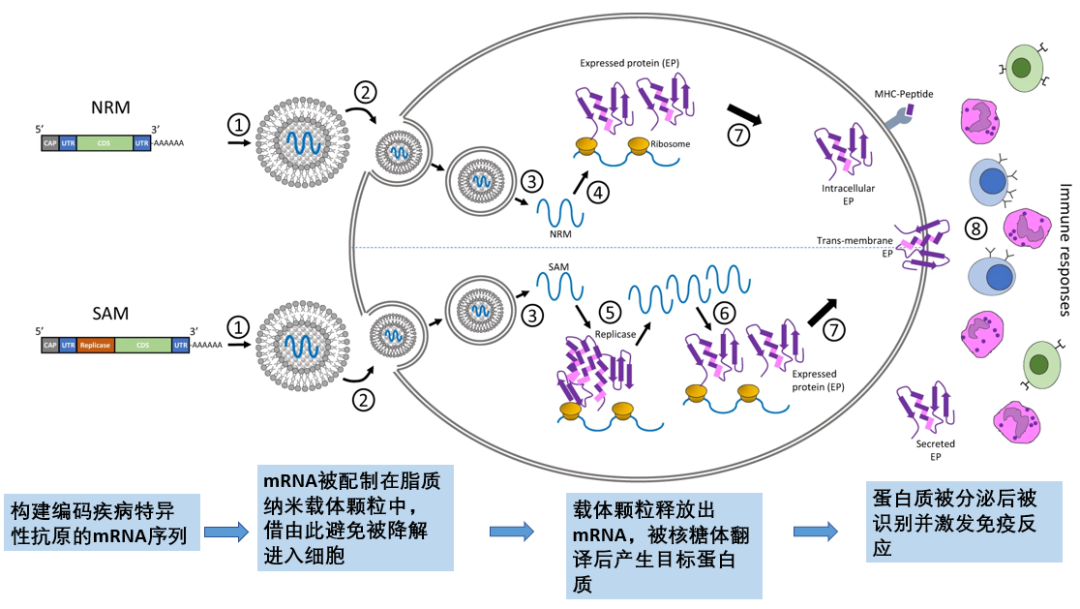
图3. mRNA疫苗的作用机制
(图片来源:https://www.nature.com/articles/s41541-020-0159-8#Fig1)
根据上述不同疫苗制备技术可以看出,传统疫苗的研发周期长,生产相对费时费力。而mRNA疫苗的优势正在于对病毒基因组进行测序之后,就可快速进入研发流程。理论上来说,在研发成功之后,它的生产流程所需要的就是组成RNA的碱基(即A、U、C和G)和酶,因此可以快速线性放大生产。辉瑞与Moderna公司对疫苗的产量预期都十分高:辉瑞表示2021年能够生产多达13亿剂疫苗,而Moderna公司则表示2021年将能在全球生产5亿至10亿剂疫苗。
但是这一切仅仅是预期。由于之前没有mRNA疫苗的上市案例,因此相关的法规、质控标准、以及运输注意事项等方面都是在摸索中前行,还存在许多未知的问题,这些无法排除的意外情况可能会造成疫苗产能与预期值存在偏差。
除了预估产量有一定差别,这两种跑在最前面的mRNA疫苗还存在如下差别:
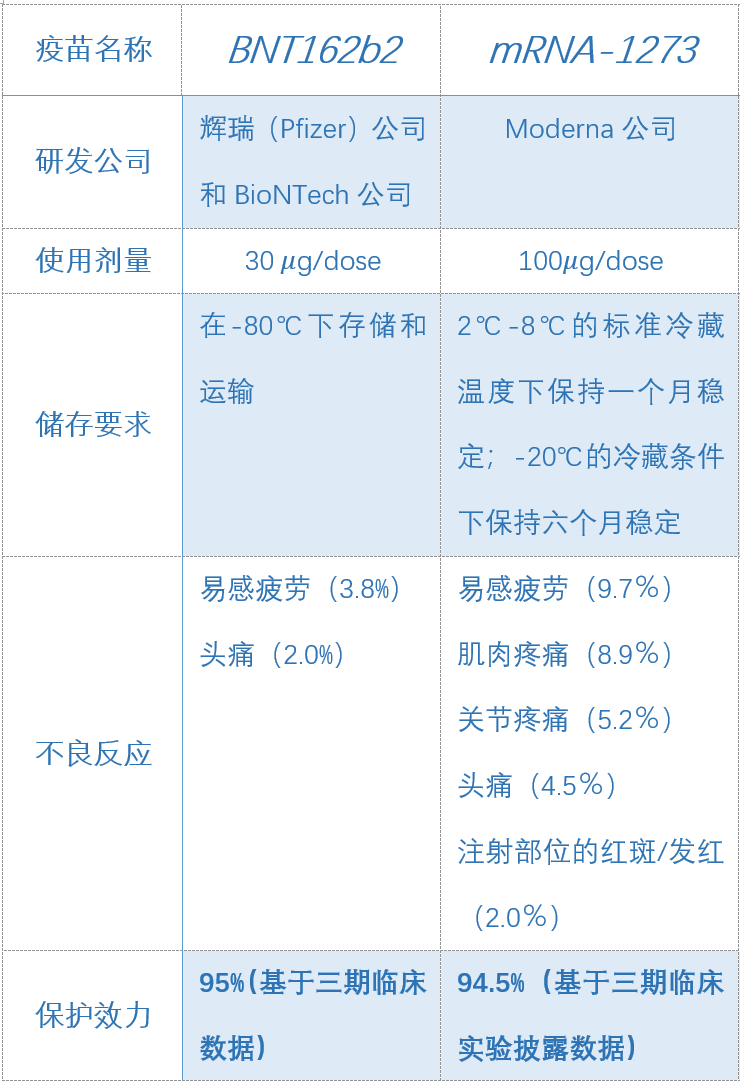
使用剂量有差异。在官方报道的临床实验数据中,辉瑞公司的BNT162b2疫苗单次注射的剂量为30μg,而Moderna公司的mRNA-1273疫苗单次注射剂量为100μg,是前者的3倍[11];
在储存和运输方面,Moderna公司称mRNA-1273疫苗稳定性优于辉瑞的BNT162b2。后者必须在-80℃下存储和运输,而前者可在2℃-8℃的标准冷藏温度下保持稳定一个月,并在-20℃的冷藏条件下保持六个月的稳定;这意味着Moderna的疫苗在储存、运输和使用方面更为便利;
在安全性方面,根据双方披露的数据来看:辉瑞公司的BNT162b2无明显的安全隐患,常见的不良反应只有易感疲劳(3.8%)和头痛(2.0%)[12];而Moderna公司也同样表示临床实验结果表明无重大安全隐患,大多数不良反应为轻度或中度,第一次给药后会出现注射部位疼痛(2.7%),第二次给药后会出现易感疲劳(9.7%),肌肉疼痛(8.9%),关节痛(5.2%) ,头痛(4.5%)和注射部位的红斑/发红(2.0%)等[8]。
在保护效力方面,辉瑞与BioNTech公司11月18日公布的三期临床数据表明,BNT162b2疫苗的有效率达到95%;Moderna公司的三期临床试验数据则表明RNA-1273 疫苗具有94.5%的保护效力。从数字上看,二者相差无几,现在还无法选出优胜者,因为二者临床试验的构建方式存在一定差异,并且目前披露出的有限的临床试验和安全性数据无法为我们提供更多的信息。
我们需要不止一个冠军
这场始于2020年初的疫情,没人能想到它的影响力会如此之大。大家都在焦急等待着有效疫苗的上市,期待着它能将我们混乱的2020拉回正轨,最近的一些关于疫苗的新闻和数据也给了我们这样的希望,各大公司和科研机构都在快马加鞭加快研发进度,所有人都将期待的眼神聚焦在终点线上,期待着领先者大步迈过终点,为我们带来好消息。但用“竞赛”来形容可能并不合适,传统疫苗和新技术到底哪种效果更好尚未可知,对疫苗安全性的考察我们仍需慎之又慎。更重要的是,我们希望不止一个胜利者冲过终点——希望有更多的疫苗可供选择,成为人类健康坚强可靠的守护者。
参考文献
[1]https://www.who.int/publications/m/item/draft-landscape-of-covid-19-candidate-vaccines
[2] Advances in mRNA Vaccines for Infectious Diseases,Front. Immunol., 27 March 2019, https://doi.org/10.3389/fimmu.2019.00594
[3] https://theconversation.com/from-adenoviruses-to-rna-the-pros-and-cons-of-different-covid-vaccine-technologies-145454
[4] https://www.pharmaceutical-technology.com/news/sinovac-vaccine-emergency-use/
[5] https://www.nature.com/articles/d41586-020-02523-x
[6] https://sputnikvaccine.com
[7] https://www.ft.com/content/96614ecd-c854-4582-a1a6-76c050c5c847
[8] https://investors.modernatx.com/news-releases/news-release-details/modernas-covid-19-vaccine-candidate-meets-its-primary-efficacy
[9] Jackson, N.A.C., Kester, K.E., Casimiro, D. et al. The promise of mRNA vaccines: a biotech and industrial perspective. npj Vaccines 5, 11 (2020). https://doi.org/10.1038/s41541-020-0159-8
[10] https://www.acsh.org/news/2020/10/21/how-pfizers-rna-vaccine-works-15104
[11] https://www.cdc.gov/vaccines/acip/meetings/downloads/slides-2020-08/COVID-07-Oliver.pdf
[12] https://www.pfizer.com/news/press-release/press-release-detail/pfizer-and-biontech-conclude-phase-3-study-covid-19-vaccine
-
康希诺生物董事长宇学峰:揭秘新冠疫苗领跑者2020-11-21
-
辉瑞宣布新消息,疫苗有效率高达95%,一举超过Moderna疫苗2020-11-19
-
特斯拉CEO马斯克确诊新冠 并表示不接受疫苗2020-11-19
-
辉瑞称其疫苗有效率达95%,明年能否用上疫苗?2020-11-19
-
钟南山说新冠病毒溯源尚未完成 大规模接种疫苗需要1至2年2020-11-17
-
特斯拉正在研发第三代疫苗打印机 未来或可打印新冠疫苗2020-11-13
-
疫苗重大进展!辉瑞宣布新冠疫苗有效性超过90%2020-11-10
-
康希诺生物重组新冠疫苗在墨西哥开展III期临床试验,多国受试者已接种2020-11-08
-
曾被紧急叫停的牛津新冠疫苗在美国恢复试验2020-10-25
-
流行病学专家吴尊友:普通人不用着急打新冠疫苗2020-10-22
-
靶向毒性Aβ的新疫苗有助于阻止阿尔茨海默病的进展2020-10-22
-
浙江绍兴率先开放新冠疫苗预约 总费用428元2020-10-21
-
国产新冠病毒疫苗如何定价?卫健委表态2020-10-20
-
疫苗能阻止疾病,为什么还有这么多怀疑?2020-10-20
-
我国新冠病毒疫苗四支疫苗已进入三期临床试验2020-10-19