五部门关于开展2024年新能源汽车下乡活动的通知
燃料电池——蓄势待发的绿色电池
燃料电池——蓄势待发的绿色电池 引言 燃料电池(FuelCell)最早可追溯到1839年英国WilliamGrove进行的水逆电解反应时所发明的技术,至于其真正的实用化,则直到
引言
燃料电池(FuelCell)最早可追溯到1839年英国WilliamGrove进行的水逆电解反应时所发明的技术,至于其真正的实用化,则直到20世纪60年代才实际应用在航天及太空上。到20世纪80年代,在环保、节能等全球议题带动下,美国、日本、加拿大、韩国及西欧各国等数百家公司及研究机构积极投入,燃料电池开始进入民用市场,到20世纪90年代后期燃料电池技术新专利不断产生。近年,在低碳经济的全球背景下,燃料电池研发和商业化进程有加快趋势。
1 定义
燃料电池是一种在等温下直接将储存在燃料和氧化剂中的化学能高效率(37~70%)地转换成化学能的电源产品;由于所使用的主要是氢气、醇类等燃料,且转动的组件极少,具有对环境负荷小(低污染)、低噪音的特点,故其不仅适合用于中央电厂和区域分散电厂发电,亦可作为交通运输工具(例如电动汽车、电动机车及电动自行车等)的动力电源,近年来,在国际领先企业的积极投入研发推动下,具有成为便携式电子产品下一代动力电池的潜力。
2 工作原理
燃料电池实质是一种电化学装置,组成与一般电池相同,其单体电池是由正负两个电极以及电解质组成。不同的是一般电池的活性物质贮存在电池内部,限制了电池容量,而燃料电池的正、负极本身不包含活性物质,只是个催化转换元件,因此,燃料电池是名符其实的把化学能转化为电能的能量转换机器。
电池工作时,负极供给燃料(氢),正极供给氧化剂(空气)。具体来说,它是利用一种叫质子交换膜的技术,使氢气在覆盖有催化剂的质子交换膜作用下,在阳极催化分解成为质子(氢离子)和电子,氢离子进入电解液中到达正极,电子不能通过质子交换膜达到正极,而是沿外部电路移向正极,用电的负载就接在外部电路中。在正极上,空气中的氧同电解液中的氢离子吸收抵达正极上的电子形成水并释放热量。
燃料电池在产生电能过程中并不会产生明火,也不需要旋转式发动机等运动部件,因此,燃料电池构造简单,能量利用率高,噪音小而且稳定。理论上,应用于汽车的燃料电池可以把氢燃料能量的60~70%转化为动能,而内燃机只能达到20~25%。
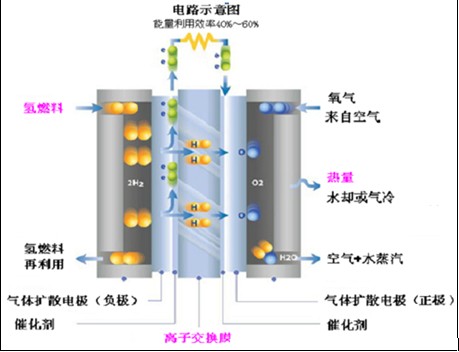
图1燃料电池工作原理示意图
3 分类
燃料电池按照不同的标准可以划分为不同的类别:如按照电池的运行机理可划分为酸性燃料电池和碱性燃料电池;按照电解质的种类可分为碱性燃料电池(AFC)、磷酸燃料电池(PAFC)、熔融碳酸盐燃料电池(MCFC)、固体氧化物燃料电池(SOFC)和质子交换膜燃料电池(PEMFC);按照燃料类型可划分氢气、甲醇、甲烷、乙烷等燃料电池;按照工作温度可划分为低温型、中温型和高温型燃料电池;按照结构类型可分为管状、平板型和单片型燃料电池等。
表1燃料电池按不同的方法分类

4 划分标准类别
按运行机理分为酸性燃料电池和碱性燃料电池
按电解质种类分为碱性燃料电池(AFC)、磷酸燃料电池(PAFC)、熔融碳酸盐燃料电池(MCFC)、固体氧化物燃料电池(SOFC)和质子交换膜燃料电池(PEMFC)
按燃料类型分为氢气、甲醇、甲烷、乙烷、甲苯、丁烯、丁烷等燃料电池
按工作温度分为低温型(温度低于200℃)、中温型(温度为200~750℃)、高温型(温度高于750℃)燃料电池
按结构类型分为管状燃料电池、平板型燃料电池和单片型燃料电池等
不同种类燃料电池之间的特性不同。常温下工作的燃料电池,如受车用动力青睐的质子交换膜燃料电池(PEMFC),这类燃料电池需要采用贵金属作为催化剂。燃料的化学能绝大部分都能转化为电能,只产生少量的废热和水,不产生污染大气环境的氮氧化物,不需要废热能量回收装置,体积较小,质量较轻。但催化剂铂(Pt)会与工作介质中的一氧化碳(CO)发生作用后产生“中毒”现象而失效,使燃料电池效率降低或完全损坏。而且铂(Pt)的价格很高,增加了燃料电池的成本。
在高温(600~1000℃)下工作的燃料电池,如熔融碳酸盐燃料电池(MCFC)和固体氧化物燃料电池(SOFC),这类的燃料电池不需要采用贵金属作为催化剂。但由于工作温度高,需要采用复合废热回收装置来利用废热,体积大,质量重,只适合用于大功率的发电厂中。
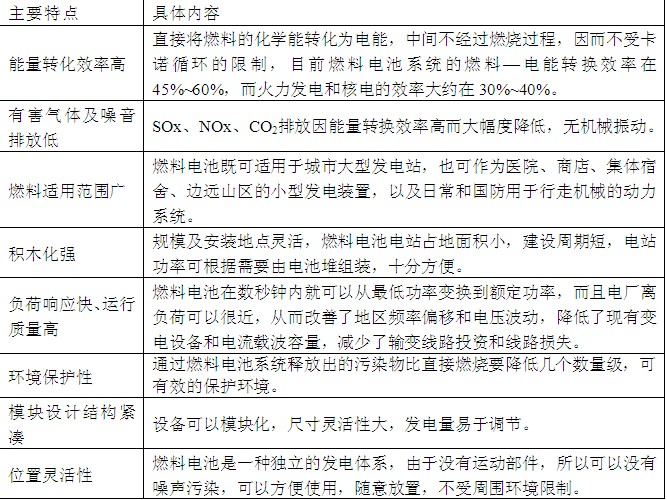
5 主要特性
传统能源利用方式主要有两大弊病:一是储存于燃料中的化学能必需首先转变成热能后才能被转变成机械能或电能,受卡诺循环及现代材料的限制,在机端所获得的效率一半以上被浪费;二是传统的能源利用方式给今天人类的生活环境造成了巨量废水、废气、废渣、废热和噪声的污染。
多年来人们一直在努力寻找既有较高的能源利用效率又不污染环境的能源利用方式,而燃料电池就是比较理想的发电技术。燃料电池十分复杂,涉及化学热力学、电化学、电催化、材料科学、电力系统及自动控制等众多学科相关理论,具有发电效率高、环境污染少等优点。
表2燃料电池主要特性
6 燃料电池发展瓶颈
燃料电池与其他动力相比虽然有许多优点,但是也面临成本过大、造价偏高的问题。例如车用质子交换膜燃料电池成本中贵金属催化剂约占40%,质子交换膜约占35%,这两者的造价都很昂贵。另外,燃料电池的启动速度与内燃机引擎还有差距,燃料电池的反应性和稳定性二者存在不可兼得的矛盾。同时燃料电池的碳氢燃料目前还无法直接利用,除甲烷外均须经转化器处理产生纯氢才可以应用。此外,储氢技术的制约和加氢充气站基础建设的不足也极大地制约了燃料电池的推广。
总而言之,燃料电池在以下几个方面有待突破。
燃料电池使用成本:(1)燃料电池使用贵金属铂作为催化,且铂极易因一氧化碳中毒丧失活性;(2)氢气制取成本高,每公斤氢气价格为汽油的数倍,储运难度大,氢气储运成本高;(3)燃料电池的稳定性、寿命、复杂路况下的性能衰减,维护费用较高。
加氢网络:氢气常温常压下是易燃易爆的气体,且很难液化。气体状态下,能量密度低(680个大气压下的氢气气体,能量密度仅为一加仑汽油液体的14%)。氢能基础设施落后,短时间内难以组成一个像加油站一样的网络。
7 结语
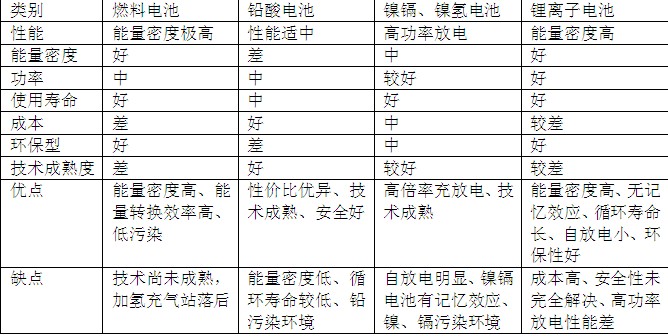
通过对比不同类型电池性能和应用后,赛迪顾问认为虽然目前铅酸、镍氢电池在动力电池领域占据主导地位,但由于污染性和续航能力等问题,传统的铅酸、镍氢电池将逐渐被淘汰。随着锂电池技术的不断成熟,制造成本和安全性能的逐渐提高,锂离子电池在未来五到十年内将是动力电池发展的主流方向。
但是,锂离子电池存在下游原料供应短缺、电池安全稳定性差等方面问题。而燃料电池是一种纯正的绿色清洁能源,可减轻温室效应使全球气候变暖,符合当前低碳经济的需要,同时氢气等燃料供给来源途径广阔,燃料电池具有很大的发展潜力。如果燃料电池在技术上有突破的话,燃料电池将有很大的发展空间。
表3燃料电池与其他动力电池比较
预计到本世纪20年代,燃料电池技术的成熟将对锂离子电池行业造成一定的冲击,而且这种技术突破在政府政策和投入支持背景下也可能比市场预期来得要早,燃料电池的商业化进程可能会加速,因此,燃料电池目前正受到企业尤其是各国政府的重视,具备较高的投资价值。赛迪顾问认为未来燃料电池行业发展在于关键技术和加氢网络等瓶颈的突破,投资重点在于燃料电池单体核心及成本占用较高的关键材料上,重点关注掌握核心技术和具备资金实力的燃料电池企业和研究机构。
上一篇:ISG型轻度混合动力汽车系统概述
-
燃料电池电动汽车的缺点2023-11-30
-
燃料电池汽车工作原理2023-11-30
-
燃料电池汽车特点2023-11-30
-
燃料电池汽车关键技术2023-11-30
-
中国氢燃料电池汽车落后国外5—10年2023-11-30
-
通用氢燃料电池汽车有望提前量产2023-11-30
-
燃料电池车,是在侮辱谁的智商?2023-11-30
-
电动车的生机远远大于燃料电池汽车2023-11-30
-
燃料电池客车最有希望率先商业化2023-11-30
-
“十三五”电动汽车展望 电池决定发展重点2023-11-30
-
燃料电池汽车前景如何2023-11-30
-
动力电池市场亟待“肃清” 新能源车企迎危机2016-06-14
-
动力电池回收缺乏标准 梯级利用将提上日程2016-06-14
-
【聚焦】低速电动车动力之争 锂电池更胜一筹?2016-06-14
-
动力电池“一刀切”的管理方式 新能源车企或难以消受2016-06-14


